光化学反应的特点
作者:上海峰志仪器 时间:2020-07-26 20:49:26浏览10643 次
信息摘要:
光化学反应的途径与产物往往和热化学反应不同。只要光的波长适当,能为物质所吸收,即使在很低的温度下,光化学反应仍然可以进行温度对光化学的影响甚微,可以忽略不计。而热化学反应对温度十分敏感。光化学反应与热化学反应动力学也不相同。反应物分子话化是通过吸收光量子而实现的。光化学反应的速率及平衡组成与吸收光强度(Ia)有关,有时与反应物浓度无关。
我们说光化学是研究光与物质相互作用的科学,如果在光的作用下,物质发生了化学反应我们称为光化学反应。光化学反应与一股热化学反应相比有许多不同之处,主要表现在,加热使分子活化时,体系中分子能量的分布服从玻尔兹曼分布:面分子受到光激活时,原则上可以做到选择性激发,体系中分子能量的分布属于非平衡分布。所以光化学反应的途径与产物往往和基态热化学反应不同,只要光的波长适当,能为物质所吸收,即使在很低的温度F,光化学反应仍然可以进行。
光化学反应系统中光化学过程可分为初级过程和次级过程。初级过程是分子吸收光子使电子激发,分子由基态提升到激发态,激发态分子的寿命一服较短。 光化学主要与低激发态有关,激发态分子可能发生解离或与相邻的分子反应,也可能过渡到一个新的激发态上去,这些都属于初级过程,其后发生的任何过程均称为次级过程。分子中的电子状态、振动与转动状态都是量子化的,即相邻状态间的能量变化是不连续的。因此分子敝发时的初始状态与终止状态不同时,所要求的光子能量也是不同的,而且要求二者的能量值尽可能匹配。
由于分子在一股条件下处于能量较低的稳定状态,称为基态。受到光照射后,如果分子能够吸收电磁辐射,就可以提升到能量较高的状态,称为激发态。如果分子可以吸收不同波长的电磁辐射,就可以达到不同的激发态。按其能量的高低,从基态往上依次称为激发态、第二激发态等,光化学研究中,把高于激发态的激发态统称为高激发态。
激发态分子的寿命般较短,而且激发态能级越高,其寿命越短,以致来不及发生化学反应,所以光化学主要与低激发态有关。激发时分子所吸收的电磁辐射能有两条主要的耗散途径:一是和光化学反应的热效应合并:二是通过光物理过程转变成其他形式的能量。
光物理过程可分为辐射弛豫过程和非辐射弛豫过程。辐射弛豫过程是指将全部或部分多余的能量以辐射能的形式耗散掉,分子回到基态的过程,如发射荧光或磷光:非辐射弛豫过程是指多余的能量全部以热的形式耗散掉,分子回到基态的过程。
决定一个光化学反应的真正途 径往往需要建立若干个对应于不同机理的假想模型,找出各模型体系与浓度、光强及其他有关参量间的动力学方程,然后考察哪个模型与实验结果的相符合程度zui高,以决定哪一个是zui可能的反应途径。
光化学反应机理的研究中常用实验方法很多。 研究中一股需要结合各种稳态,瞬态的光谱仪器,分析光化学研究反应过程的中间体,如采用同位素示踪原子标记法等方法可以更方便地确定反应历程。在光化学中zui早采用的荧光猝灭法仍是一种简单有效的方法。 这种方法是通过被激发分子所发荧光,被其他分子猝天的动力学测定来研究光化学反应机理的。由于吸收什么波长的光往往是由分子中某个基团的性质决定的,所以光化学可以使分子中某特定位置直接发生化学反应,对于那些缺乏选择性热化学反应或者反应发生后的体系被破坏的热化学反应更为可贵。光化学反应的另特点是 用光子作为反应试剂,-且被反应物吸收后,不会在体系中留下其他新的杂质,因而可以看成是“zui纯”的试剂。所以和热化学方法相比,光化学合成方法具有反应速率快、产物单一和副产物少等优点。
光化学反应是自然界 十分重要的现象,可以说有光的地方就有光化学反应的发生。地球与行星的大气现象,如大气构成、极光、辐射屏蔽和气候等,均和大气的化学组成与对它的辐照情况有关。处于高空处大气的原子与分子吸收太阳辐射后会发生光化学反应。导致它和在地表上我们熟知的主要由氮气与氧气组成的空气完全不同。
解了光化学以后,另一个和光化学休威相关的名词是光物理。了解具体的光化学过程必须要熟悉激发态的物理性质。
所以说它们二者之间互相沙透,互相补充,特别是近30年来,由于激光的间世,光学的面貌发生了深刻的变化,光物理的研究内容也从传统的光学与光谱学迅速扩展到光学与物理其他分支学科的交汇点。
诸如激光物理、非线性光学、高分辦率光诺学、强光光学和量子光学正不断趋于完善和成熟,有的则正在积累形成新的分支学科,如光子学、超快光谱学和原子光学等,光物理与化学、生物学、医学及生命科学的交叉也越来越广泛和深人。光物理学中的新理论、新概念和新方法已成为激光、光纤通信等高技术产业发展的重要依托。
光化学有两条基本定律,光化学定律是在1818年由Grothuss和Draper提出:只有被系统吸收的光才可能产生光化学反应。不被吸收的光(透过的光和反射的光)则不能引起光化学反应。只有为反应所吸收的辐射光,才能有效地产生光化学变化。光化学第二定律是在1908 ~ 1912年由Esinstein 和Stark提出:在初级过程中,一个光量子活化个分子。
光化学反应与一 般热化学反应相比有许多不同之处,主要表现在:热化学反应中,加热使分子活化时,体系中分子能量的分布服从玻尔数曼分布。
面光化学反应中,分子受到光徽活时,原则上可以做到选择性激发(包括能量跃迁值的选择,电子激发态模式的选择等),体系中分子能量的分布属于非平衡分布。
所以光化学反应的途径与产物往往和热化学反应不同。只要光的波长适当,能为物质所吸收,即使在很低的温度下,光化学反应仍然可以进行温度对光化学的影响甚微,可以忽略不计。而热化学反应对温度十分敏感。
光化学反应与热化学反应动力学也不相同。反应物分子话化是通过吸收光量子而实现的。光化学反应的速率及平衡组成与吸收光强度(Ia)有关,有时与反应物浓度无关。
温度对光化学反应儿乎设影响。热反应的吉布斯自由能△G<0,而光化学反应的吉布斯自由能可能△G>0.热化学反应的速率常数比较大,面光化学反应的速率常数很小,有的时候近似于0.
光化学反应速率的平衡
光化学反应跟热化学反应不同,光化学反应是-个缓慢的过程。从本质上说光化学反应是一个对峙反应。在反应发生的正反两个方向,只要有一个方向是光化学反应,则其平衡即称为光化学平衡。井且光化学平衡的浓度与反应物吸收光的强度成正比。下式为一个简单分子A的光聚合反应。A可以在光照的作用下聚合生成聚合体A2,生成的A2也可以分解为A2的浓度正比于光照的强度。
hv
2A↔A2
[A2]∝Ia
在光化学反应速率中反应速率常数正比于光强度,也就是说跟吸收光的强度有关。即: r=kIa其中,Ia为吸收光速率。在光化反应动力学中,用下式定义光化学反应量子产率更合适:
r
∮=一
Ia
式中,r为反应速率,用实验测量: I,为吸收光速率,用露光计测量。
光敏反应
有些物质对光不敏感,不能直接吸收某种波长的光而进行光化学反应。如果在反应体系中加人另外一种物质,它能吸收这样的辐射,然后将光能传递给反应物,使反应物发生作用,而该物质本身在反应前后并未发生变化,这种物质就称为光敏剂,又称感光剂。光敏反应就是由光敏剂引发的反应。它的概念有点类似我们熟悉的催化剂。
例如:
H2+hv→2H
这个反应可以用Hg为光敏剂。
CO2=H2O→02 +(C6H12O6)n
这是我们熟悉的光合作用,反应中叶绿素为光敏剂。
光化学的量子效率、量子产率和能量转化效率
为了衡量一个光量子引致指定物理或化学过程的效率,在光化学中定义了量子效率。量子效率可以定义为生成产物的分子数与吸收的光子数的比值,也可以定义为生成产物的物质的量与吸收光子的物质的量的比值。可以表示如下:
生成产物的分子数 生成产物的物质的量
∮=一一一一一一一一一=一一一一一一一一一一
吸收的光子数 吸收光子的物质的量
量子效率∮是光化学反应中一个很重要的物理量,可以说它是研究光化学反应机理的敲门砖,可为光化学反应动力学提供许多信息。当∮>1,是由于初级过程活化了一个分子,而次级过程中又使若干反应物发生反应。如: H2+C2I→2HCI 的反应,1个光子引发了一个链反应,量子效率可达106次方。当∮<1,是由于初级过程被光子活化的分子尚未来得及反应,便发生了分子内或分子间的传能过程而失去活性.
(2)量子产率(quantum yield)
发生反应的分子数 发生反应的物质的量
∮=一一一一一一一一一=一一一一一一一一一一
吸收的光子数 吸收光的物质的量
由于受化学反应式中计量系数的影响,量子效率与量子产率的值有可能不等,例如,下列反应的量子效率为2,量子产率却为1.一般也用符号∮表示,也有很多书并不区分量子效率和量子产率。
2HBr+hv→H2+Br2
(3)能量转化效率
对一定波长的单色光进行的光化学反应,能量转化效率可以表示如下:
△rGm∮
η=一一一一
Ev
式中,△rGm为激发态的吉布斯自由能:∮为将光子转化为化学产物的量子产率,Ev为人射光的总辐照度,W/m2。
值得注意的是光化学反应的量子效率可以小于 1,也可以大于1,但无论量子效率是小于1,还是大于1.其能量转化效率都不能超过1。
生活中的光化学现象
人类开始系统地进行光化学研究已有近百年的历史,然而光化学形成化学的一个新兴分支学科则还不是半个世纪。光化学学科在20世纪60年代形成后,其发展十分迅速。在光化学形成化学的一个独立分支学科之前,高等学校的光化学课程一直归属于物理化学中动力学的教学内容。
20世纪60年代激光的发现和70年代初发生的石油危机,大大促进了化学和物理交叉学科的发展。现代光化学或称激发态化学的研究,早已不仅局限于化学和物理领城的交叉,它正在向材料科学、生命科学、环境科学、能源科学,甚至信息科学等诸多技术领域渗透,形成诸如生物光化学、环境光化学、光电化学、超分子光化学、光催化和光功能材料等新的分支和边缘学科。
因此可以说,光化学现在已经是化学与材料科学、能源科学、生命科学、环境科学等诸多科技领城相关的一门基础学科。按照普遍的定义,光化学是研究物质(原子、小分子)因受光的影响而产生性化学效应的一个学科。
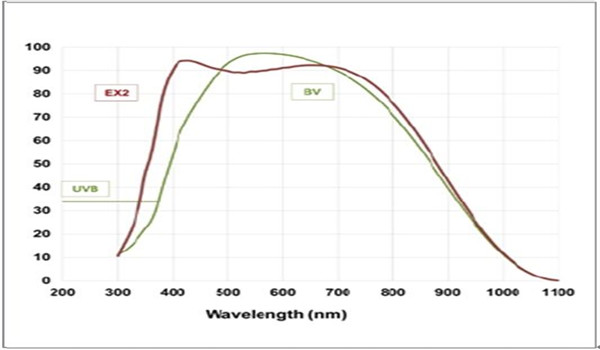
由于历史的和实验技术方面的原因,光化学所沙及的光的波长范围为100~ 1000nm,即由紫外至近红外波段。比紫外波长更短的电磁辐射,如X或y射线所引起的光电离和有关化学变化,则属于辐射化学的范畴。至于远红外或波长更长的电磁波,L般认为其光子能量不足以引起光化学过程,因此不属于光化学的研究范畴。近年来观察到有些化学反应可以由高功率的红外激光所引发,将其归属于红外激光化学的范畴。
人们对日常生活中的光化学现象早就观察到了。例如,染过色的衣服经光的照射会褪色.这是因为染色衣物经多次水洗和长期日晒,使衣物上的染料发生光分解和光氧化,从而使衣物出现了褪色现象。这种现象不是一蹴而就,而是逐步发生的,其过程是比较复杂的。这正是光化学反应的特点。当阳光照射在染色衣物上时,光能激发了染料分子使之活化。活化的染料分子更容易与其他物质发生反应,例如跟空气中的氧反应,若有水分子的存在则会进一步加剧化学反应的程度。由于染料分子的氧化或还原反应,而使染色衣物发生褪色。如用偶氮染料染色的棉纤维织物经日晒褪色,是因为氧化作用的结果,而用同种染料染色的蛋白纤维织物经日晒褪色,却是还原作用的结果。又如,变色镜片是在普通玻璃中加入了适量的溴化银和氧化铜的微小品粒。当强光照射时,溴化银分解为银和溴。分解出的银的微小晶粒,使玻璃星现暗棕色。当光线变暗时,银和溴在氧化铜的催化作用下,重新生成澳化银,于是,镜片的颜色又变浅。具体反应如下:
hv
2AgBr → 2Ag+Br2
CuO
2Ag+Br2 → 2AgBr
植物受到光照会生长 (光合成), 即我们常说的光合作用。光合作用是指绿色植物通过叶绿体,利用光能,把二氧化碳和水转化成储存着能量的有机物,并且释放出氧的过程。我们每时每刻都在吸人光合作用释放的氧,我们知道在地球上的生命是依靠太阳的能量生存着,而光合作用是唯-能捕获此能量的重要生物途径。所以,光化学过程是地球上zui普遍、zui重要的过程之一,不论是通过理论还是实验技术的方法,与光合作用相关的光化学研究一直是一个极活跃的领城。
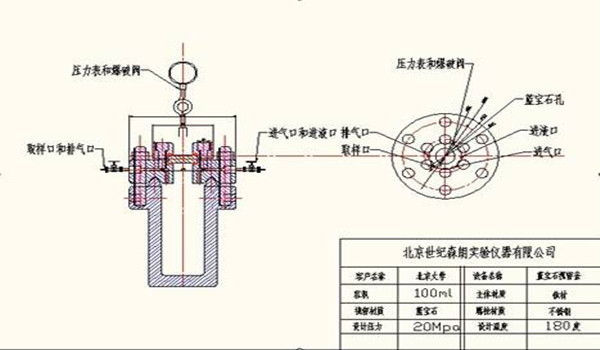
上海峰志仪器有限公司销售多种波段的光化学反应器,有254nm、365nm、455nm、555nm、660nm等多种波段,还有led 16通道平行光光化学反应器。









 添加微信咨询!
添加微信咨询!